






Ключевыми свойственными показателями считаются: усиленная стойкость ароматической системы, а также, невзирая на ненасыщенность, тенденции к реакциям замещения, а не соединения. К ароматическим углеводородам относится простейшее органическое вещество бензол (фениловый водород) \(C_6H_6\), а также ряд гомологов и производных, включая химические соединения с некоторым количеством бензольных ядер, такие как гексален (\(С_{10}Н_8\)), тритан (\(C_{19}H_{16}\)) и так далее.
Фениловый водород (\(C_6H_6\)) считается самым первым ареном, который был открыт наукой. Химическая формула фенилового водорода была открыта английским физиком-экспериментатором и химиком Майклом Фарадеем еще в 1825 году. Фарадей выделил бензол из светильного газообразного вещества (продукта термического разложения китового жира).
В 1833 году немецкий химик Эйльхард Мичерлих в чистом виде осуществил получение бензола сухой перегонкой бензойной кислоты (\(C_6H_5COOH\)) с излишком гидроксида кальция (\(Ca(OH)_2\)), а также он осуществил приготовление нитробензола (\(C_6H_5NO_2\)) и азобензола (\(C_{12}H_{10}N_2\)). Эйльхард Мичерлих дал ему фениловому водороду наименование «бензин», однако немецкий химик Юстус фон Либих со временем переименовал фениловый водород в «бензол» (окончание происходит от немецкого слова масло – Öl)
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Дальше постепенно число открытых химических соединений, схожих по структуре и химическим свойствам с фениловым водородом, постоянно возрастало. Большое количество данных соединений обладали приятным ароматическим свойством, что и предоставило основу для немецкого химика-органика Фридриха Августа Кекуле дать наименование этим соединениям «ароматические».
Значительную роль в определении построения фенилового водорода сыграл немецкий химик Фридрих Август Кекуле. Он представил для бензола формулу 6-тичленного цикла с тремя двойными взаимосвязями. Однако данная формула не осуществляла объяснения, по какой причине не присутствует два изомера, к примеру, 1,2-диметилбснзола с разным расположением метильных групп по двойной взаимосвязи, если выходить из представленного состава с замкнутыми двойными взаимосвязями.
Как было определено другими учеными, данные 1,2-дизамещенные гомологи фенилового водорода являются одним соединением, что отрицает взгляды об определенной локализации двойной взаимосвязи:
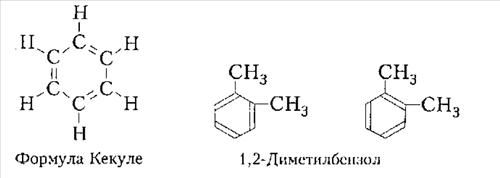
Рисунок 1.
Для пояснения неимения зафиксированных ненасыщенных взаимосвязей в молекулярной основе фенилового водорода Фридрих Август Кекуле в 1872 году предложил концепцию об осцилляции, или переходном процессе, двойных взаимосвязей. Данное пояснение говорит о равнозначности углеродных атомов в молекуле фенилового водорода, так как все атомы связаны с соседними углеродными атомами простыми и двойными взаимосвязями, относительно быстро меняются местами (осциллируют).
Несимметричные 1,2-дизамещенные производные фенилового водорода, в соответствии с формулой Фридрих Кекуле, обязаны присутствовать как 2 разных изомера – I и II:

Рисунок 2.
Но, в действительности, постоянно присутствует только 1 орто-изомер. Для устранения данного отклонения Фридрих Кекуле сделал предложение, что двойные взаимосвязи в 1,3,5-циклогексатриене постоянно осуществляют перемещения, и оба изомера практически мгновенно преобразовываются один в одного (теория «осцилляции валентности»):
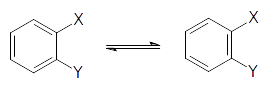
Рисунок 3.
Концепция Фридриха Кекуле об осцилляции ненасыщенных взаимосвязей некогда доказана итогами озонирования углеводородов ароматического ряда:
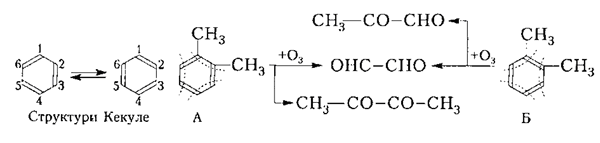
Рисунок 4.
К примеру, изомер A обязан формировать этандиаль (\(C_2H_2O_2\)) и диметилглиоксаль (\(С_4H_6O_2\)) в соотношении 2 к 1, а изомер Б обязан формировать этандиаль и 2-оксопропаналь (\(C_3H_4O_2\)) в соотношении 1 к 2. В действительности при озонировании углеводородов ароматического ряда формировались все 3 продукта с соотношением 2-оксопропаналь (\(C_3H_4O_2\)): этандиаль (\(C_2H_2O_2\)): диметилглиоксаль (\(С_4H_6O_2\)) 3: 2: 1, что говорило бы на пользу присутствия в изначальной смеси одинаковых величин состава A и Б.
Как со временем прояснилось составов фенилового водорода типа A и Б нет, а итоги озонирования углеводородов ароматического ряда показывают только равнозначность всех 6 углеродных атомов в ядре бензола.
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
Помимо формул Фридрих Кекуле для фенилового водорода было осуществлено большое количество предложений формул. Среди тех, которые достойны упоминания химические формулы:
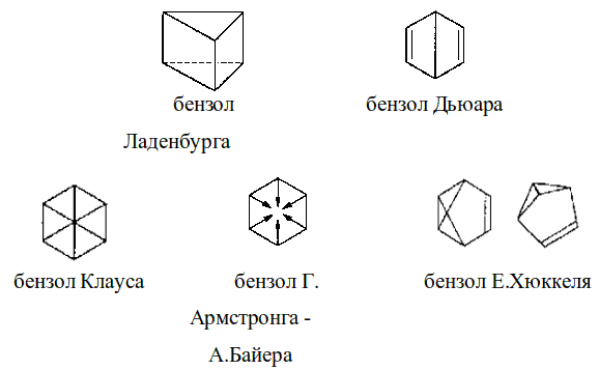
Рисунок 5.
Необходимо заметить, что в последнее время соединения подобно строений Джеймса Дьюара, Альберта Ладенбурга, Эриха Хюккеля синтезированные в реальности в виде валентных изомеров фенилового водорода. Таким образом, при ультрафиолетовом облучении фенилового водорода в соответствии с волновой длиной формируется бензвален (строение Эриха Хюккеля) либо бицикло[2.2.0]гекса-2,5-диен (бензол Дьюара), который при последующем облучении преобразовывается в призман (призматическая форма фенилового водорода Альберта Ладенбурга):

Рисунок 6.
Наведенные валентные изомеры фенилового водорода обладают отличием один от одного числом π-взаимосвязей и их положением, не обладают плоской структурой, а также обладают неустойчивостью при нагреве и легко осуществляют изомеризацию к первоначальному фениловому водороду.
Из до электронных описаний построения фенилового водорода ближе к нынешнему пояснению был И.Тиле в 1899 году. Этот ученый применил теорию «частичных» валентностей. В соответствии с данной теорией в ненасыщенных химических соединениях все углеродные атомы обладают частичной независимой валентностью. И в ядре бензола они «уходят» к одинарной взаимосвязи между собой, что осуществляет выравнивание разности между простыми и двойными взаимосвязями.
На стыке XIX и XX столетия было представлено множество научных трудов по химической направленности по ароматическим соединениям. Но неясным было ключевой вопрос о взаимной связи построения фенилового водорода, а также его химических свойств. Невзирая на присутствие 3-х двойных взаимосвязей, в противовес алкенам, фениловый водород с трудом осуществляет вступление в реакции соединения, а намного легче в реакции замещения. Таким образом, фениловый водород не осуществляет присоединение галогенов, помимо хлора, воды и серной кислоты.
Бензол обладает устойчивостью к действию окислителей, и не производит обесцвечивание раствора \(KMnO_4\). Фениловый водород является значительно устойчивым к температуре, нежели алифатические триены. Он переносит нагревание до температуры +900°C. Помимо этого, присутствие бензольного кольца в молекуле значительнее, нежели алкильных либо алкенильных остатков, воздействует на иные функциональные группы. К примеру, под воздействием ядра бензола фенолы демонстрируют высокую кислотность, нежели алифатические спиртовые составы, а ароматические амины – малые основы сравнительно с алифатическими аминами. Пояснение данных фактов оказалось доступным лишь после определения структуры фенилового водорода, привлекая квантово-механических методы.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




