






Соединениями с конденсированными ядрами бензола (полициклическими ароматическими углеводородами) именуют такие соединения, которые включают общие углеродные атомы. Структура данных соединений бывает:
Полициклические ароматические углеводороды – это органические соединения, для которых типично присутствие в химическом составе двух и больше конденсированных колец бензола. Ключевыми представителями конденсированных полициклических ароматических углеводородов являются:
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
Тип влияния полициклических ароматических углеводородов на живые организмы в основном находится в зависимости от состава непосредственно углеводорода, а также обладает возможностью изменений в достаточно обширном диапазоне. Большое количество данных углеводородов считаются сильными химическими канцерогенами. Некоторые соединения обладают очевидными канцерогенными, мутагенными, а также тератогенными свойствами.
Простейшим и важнейшим представителем данной категории химических соединений считается нафталин, который является твердым кристаллическим веществом с типичным запахом. В том числе, есть иное не менее важное бициклическое вещество, которое аналогично нафталину – это азулен (\(C_{10}H_8\)), являющийся изомером нафталина. Азулен содержит конденсированную систему из пяти и семи членного цикла.
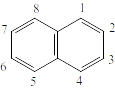
Рисунок 1. Нафталин.
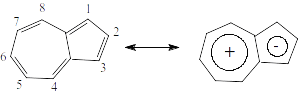
Рисунок 2. Азулен.
Открытие нафталина было осуществлено в 1819 году, в каменноугольной смоле. Его открытие произведено раньше бензола. Элементарный состав нафталина (\(C_{10}H_8\)) был определен российским химиком Александром Абрамовичем Воскресенским в 1838 году. Состав нафталина до этого времени был неизвестен, однако обладал большим значением для разрешения вопроса об углеродном атомном весе. Непосредственно структуру нафталина установил немецкие химики-органики Эмиль Эрленмейер и Карл Гребе, в ходе своих исследований в 1866-1868 годах.
В промышленном производстве нафталин получают из каменноугольной смолы, которая является продуктом коксования каменного угля. Содержание нафталина в каменноугольной смоле составляет примерно 10%. В том числе, нахождение нафталина отмечается в тяжелой смоле пиролиза. Еще одним методом добычи нафталина в промышленности считается деалкилирование его алкилпроизводных. Синтетическим образом получение нафталина можно осуществить, к примеру, из ацетилена следующими методичными реакциями:
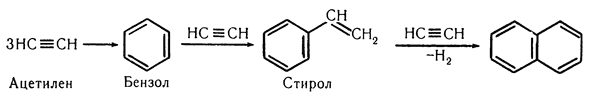
Рисунок 3.
Данное синтезирование единовременно считается подтверждение состава нафталина. В молекуле нафталина осуществляется нумерация атомов углерода. Ее осуществляют по часовой стрелке, как отражено на рисунке 1. Положение углеродных атомов 1,4,5,8 отмечают литерой α и именуют альфа-положениями. В свою очередь, положение углеродных атомов 2,3,6,7 отмечают литерой β и именуют бета-положениями.
Молекула нафталина обладает 10 атомами углерода. Данные атомы находятся в одной плоскости и расположены в углах двух связанных друг с другом (конденсированных) ядер бензола. Углеродные атомы в нафталиновой молекуле присутствуют в sp2-состоянии. В данном состоянии все атомы углерода обладают еще одним р-электроном. Таким образом, молекула нафталина содержит 10 р-электронов, обладающие видом объемных восьмерок, обоюдно полярные спины, а также параллельные оси.
Все данные p-электроны осуществляют взаимодействие с аналогичными электронами соседствующих углеродных атомов. В итоге все 10 р-электронов обоюдно осуществляют перекрытие друг с другом, организовывая, вместе с тем, единую электронную орбиталь. Данная орбиталь осуществляет охват всех 10 углеродных атомов и находится за молекулярной плоскостью:
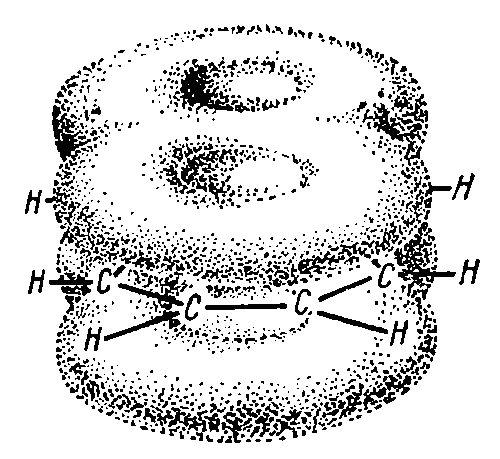
Рисунок 4.
Данную электронную орбиталь возможно исследовать как комплекс двух секстетов пи-электронов, отчасти перекрывающиеся, а также обладающие двумя общими пи-электронами.
Рентгенодифракционный анализ указывает, что в нафталиновой молекуле, в противовес фениловому водороду, промежутки между атомами углерода неэквивалентны. Действительно, рентгеноструктурные сведения указывают самое слабое пи-взаимодействие двух узловых C-атомов общей грани ядер бензола с соседствующими атомами (максимальная длина взаимосвязи 0,143 нанометров указывает, что порядок взаимосвязи минимальный):
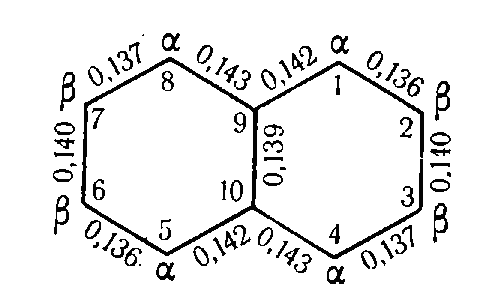
Рисунок 5.
Как показано на диаграмме нафталиновой молекулы, взаимосвязи между углеродными атомами 1-2 по длине более схожи на двойные, нежели взаимосвязи меж атомами 2-3. В свою очередь, взаимосвязи между атомами 1-2 и 3-4 в некоторой мере являются подобными сопряженной системе взаимосвязей 1-3.
По причине разного промежутка между атомами углерода пи-электронное облако в нафталиновой молекуле расположено хоть и симметрично, но прерывистым образом, что вызывает прерывистость расположения в его молекуле. На альфа-атомах углерода электронная плотность выше, нежели на бета-атомах. Самая маленькая симметрия всех конденсированных ядер бензола в нафталиновой молекуле отражается на показателях свободной валентности, а также на кратности взаимосвязей.
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Среди трициклических систем ароматическими считаются системы, которые аналогичны 14-аннуленов – фенантрен, а также антрацен (\(C_{14}H_{10}\)). Фенантрен – трициклический ароматический углеводород, нерастворим в воде, а растворим в органических растворителях. Антрацен не растворяется в воде, а растворяется в ацетонитриле (\(CH_3CN\)) и ацетоне (\(C_3H_6O\)), при нагреве растворим в фениловом водороде.
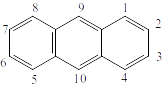
Рисунок 6. Антрацен.
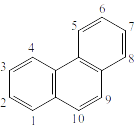
Рисунок 7. Фенантрен.
Все плоские конденсированные системы, обладающие совместными атомами для двух циклов, осуществляют подчинение правилу Эриха Хюккеля. Образцом данных систем считается тетрацен (нафтацен, \(C_{18}H_{12}\)), пентацен (\(C_{22}H_{14}\)), а также бифенилен, трифенилен и прочие конденсированные углеводороды:
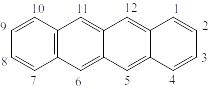
Рисунок 8. Тетрацен. Четырех циклический представитель аценов.
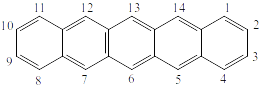
Рисунок 9. Пентацен.
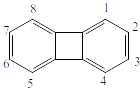
Рисунок 10. Бифенилен.
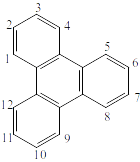
Рисунок 11. Трифенилен.
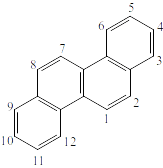
Рисунок 12. Хризен (\(C_{18}H_{12}\)).
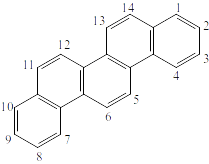
Рисунок 13. Пицен (\(C_{22}H_{14}\)).
В свою очередь, соединения, которые обладают атомами, общими для трех циклов не зависят от правила Эриха Хюккеля. Таким образом, правило Эриха Хюккеля не выполняется у аценафтилена, пирена и перилена, которые обладают соответствующе двенадцатью, шестнадцатью и двадцатью пи-электронами, поскольку формула [4n+2] не выполняется, хоть данные соединения, в том числе, считаются ароматическими:
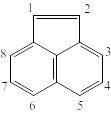
Рисунок 14. Аценафтилен (\(C_{12}H_8\)).
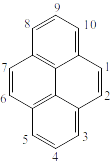
Рисунок 15. Пирен (\(C_{16}H_{10}\)).
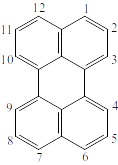
Рисунок 16. Перилен (\(C_{20}H_{12}\)).
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




