






Сульфонирование массово применяется в промышленности для синтезирования органических пигментов, активно-поверхностных веществ и прочих активных связей. Сульфированию подвергаются в основном ароматические соединения; получающиеся продукты – арилсульфокислоты. Чаще всего сульфонирование вызывает смесь изомеров, отношение которых находится в зависимости от характера заменителя в ароматическом кольце, сульфирующего реагирующего агента, условий реакции.
Сульфирование является одной из важных реакций органического синтеза и массово применяется в лабораториях, а также в производственных процессах для химического прорабатывания алифатических и ароматических углеводородных веществ в переходные продукты разного построения, в том числе с целью придания окончательным продуктам синтеза кислотных характеристик и возможности растворяться в воде.
По реакции сульфонирования в ароматические связи возможен ввод функциональной группы органических соединений, являющейся сильным электроноакцептором \(–SO_2OH\). В роли сульфирующего реактанта применяют, зачастую, концентрированную серную кислоту, купоросное масло, в том числе олеум. Реакция бензола с серной кислотой осуществляется достаточно медленно.
Агентами сульфирования являются:
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
На сегодняшний день отсутствует общее мнения по отношению подлинной природы электрофильного реагента сульфонирования. Информация кинетических исследований не предоставляет единого ответа на данный вопрос, так как в водной и безводной серной кислоте присутствует огромное количество потенциальных электрофильных реагентов. Условная концентрация данных реагентов находится в зависимости от соотношения \(H_2O – SO_3\).
Механизм реагирования сульфонирования является аналогичным, которые происходит в реакции ввода нитрогруппы \(–NO_2\) в молекулы органических соединений. Первоначально одна молекула \(H_2SO_4\) осуществляет протонирование иной молекулы. Далее, отщепляется вода и образовывается необычно реакционно-способный катион. Он осуществляет присоединение к углеродному атому ароматического цикла с образованием σ-комплекса, быстро разлагающегося с утратой протона и воспроизведением ароматической структуры.
1. Концентрированная серная кислота.
Если серная кислота сконцентрирована менее 80%, в основном, осуществляется установка таких равновесий:
\(H_2 SO_4+H_2 SO_4↔H_3 SO_4^++HSO_4^-\)
либо
\(H_2 SO_4+H_2 SO_4↔SO_3+H_3 O^++HSO_4^-\)
Когда серная кислота сконцентрирована в пределах 85-98%, ее состояние, как правило, осуществляется описанием следующих формул:
\(3H_2 SO_4↔H_2 S_2 O_7+H_3 O^++HSO_4^-\)
либо
\(H_2 SO_4+H_2 SO_4↔S_3+H_3 O^++HSO_4^-\)
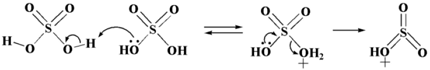
Рисунок 1.
2. Олеум. В стопроцентной серной кислоте и в олеуме кроме \(H_2S_2O_7\) присутствуют и прочие полисерные кислоты: \(H_2S_3O_{10}\); \(H_2S_4O_{13}\)и так далее. Это осуществляет существенно затруднение интерпретировать данные по кинетике сульфонирования. В олеуме темпы сульфонирования быстро растут.
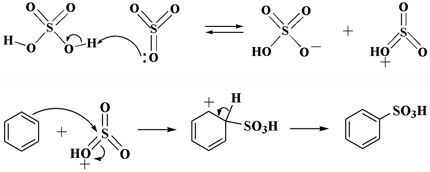
Рисунок 2.
Сульфонирование возможно осуществить при помощи олеума: растворного состав \(SO_3\) в сконцентрированной серной кислоте. В данной ситуации, катионная электрофильная частица возникает, когда протонируется сульфотриоксид серной кислотой. Непосредственно \(SO_3\) считается активнейшим электрофилом в числе сульфирующих реагентов.
Возникающие сульфокислотные соединения считаются достаточно сильными, так же как и серная кислота, в том числе, сильнее соляной кислоты. Принимая во внимание данное обстоятельство, выделение сульфокислотных соединений возможно в виде солей натрия, возникающих как осадки кристаллов при воздействии изобилия \(NaCl\).
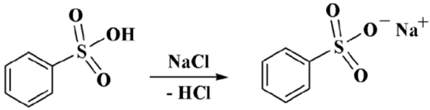
Рисунок 3.
Пара-толуолсульфонатная (тозилатная) группа OTs считается важнейшей составляющей в химических реагированиях подмены, так как это одна из лучших отходящих групп. Ее ввод возможно осуществить посредством органического соединения, хлорангидрид пара-толуолсульфокислоты. Данное соединение является реагентом для создания производных этой сульфокислоты при реакциях с соединениями разных классов.
Тозилхлорид возможно получить сульфонированием толуола сульфурилоксихлоридом. В данной реакции формируется, как правило, орто изомер хлорангидрида, отделение которого возможно перегонкой.
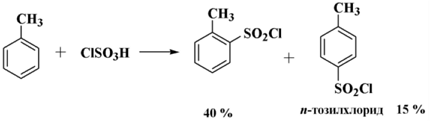
Рисунок 4.
Для сульфонирования хлоросульфоновой кислотой нет необходимости применять катализ кислотой Льюиса, поскольку данная кислота считается достаточно сильной и осуществляет протонирование самостоятельно, образовывая электрофилы, имеющие свободную орбиталь на внешнем электронном уровне. Это поясняет, по какой причине, при осуществлении замещения производит отход группа OH, а не атомная частица хлора. Итогом реакции считается хлоросульфирование, а не сульфонирование.
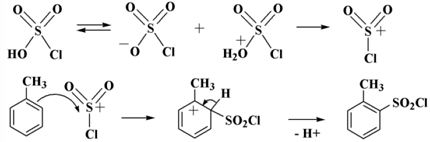
Рисунок 5.
Иным традиционным методом демонстрации термодинамического контроля считается сульфонирование нафталина. Сульфонирование нафталина серной кислотой осуществляется проще, нежели бензола, а природа продуктов подмены, в том числе, находится в зависимости от критериев осуществления реакции.
В относительно мягких критериях возникает лишь 1-нафталинсульфокис (выход 96%), при температурных параметрах около +80°C. Данным критериям соответствует сульфонирование нафталина хлорсульфоновой кислотой, которая является токсичной, либо раствором \(SO_3\) в дихлорэтане с температурными показателями от 0°C до минус 10°C.
С более строгими критериями, при температурных показателях около +160°C (термодинамический контроль) стабильнее 2-нафталинсульфокислота (выход 85%). В данных критериях 1-нафталинсульфокис, образующийся более быстро благодаря невысокой энергии перехода соответствующего σ-комплекса, под воздействием \(H_2SO_4\) перегруппируется в термодинамически стойкую 2-нафталинсульфокислоту.
Это осуществляется исходя из более низкого устойчивого состояния 1-нафталинсульфокиса, а также отчасти определено взаимным воздействием с водородом в восьмом положении нафталинового ядра:
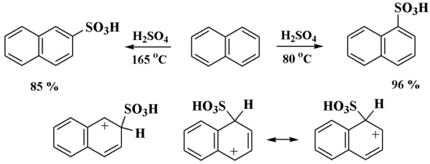
Рисунок 6.
Ароматические амины, являющиеся производными аммиака, в молекуле которого некоторое количество атомов водорода замещены на углеводородные радикалы, в том числе, возможно осуществлять сульфирование серной кислотой. Сульфонированием ароматических аминов получают амино-сульфокислоты.
С учетом того, что при данных критериях амин обязан располагаться в протонированном виде, а аммониевая группа имеет характеристики мета ориентирующего заменителя, возможно предположить формирование мета сульфокислоты. Но итогом данного взаимного воздействия становиться формирования парааминообензолсульфокислоты.
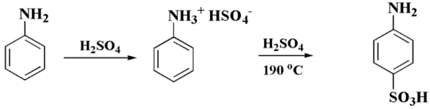
Рисунок 7.
Пояснением данного обстоятельства является присутствие в растворе реакции небольшого числа свободного амина. В частности он, как активный нуклеофил и осуществляет взаимодействие с электрофилами с формированием япара подмененного продукта. Но определенная часть научных деятелей имеют мнение, что реакция осуществляется благодаря формированию N-сульфопроизводной, которая при нагреве перегруппируется в C-подменяемую кислоту.
Аммониевая группа \(NH_{3+}\) имеет отношение к сильным электро-акцепторным заменителям, которые порождают быстрое сдерживание реакции сульфонирования, а также направляющим входящий электрофильные частицы в метаположение.
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Сульфонирование в π-положение бензольного кольца анилина считается, очевидно окончательным итогом некоторого количества конвертируемых процессов сульфонирования-десульфонирования, так как параизомер аминобензол сульфокислоты являются более устойчивыми в термодинамическом плане. Данная правомерность встречается и при сульфонировании иных ароматических аминов. Данным способом осуществляют получение некоторого количества важнейших амино-сульфокислот нафталина в промышленности.
Сульфохлорирование ацетанилида хлорсульфоновой кислотой вызывает формирование хлорангидрида π-ацетаминобензол сульфокислоты. После чего получают сульфаниламидные препараты, которые являются противомикробными средствами. Большое количество из данных веществ со средины XX столетия применяются в качестве антибактериальных препаратов.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




