






Простые эфиры относительно большого количества химических реактивов довольно инертные вещества. Эфирная взаимосвязь не подчиняется влиянию восстановителей, окислителей, оснований. Простые эфиры нет возможности осуществить расщепление: сложными гидридами алюминия (\(AlH_3\)), гидридами бора, амидами и гидридами щелочных металлов, металлоорганическими веществами.
Простые эфиры обладают следующими свойствами:
К примеру, простые эфиры тетраметиленоксид (\(C_4H_8O\)), этоксиэтан (\(CH_3-CH_2-O-CH_2-CH_3\)), диоксан (\(C_4H_8O_2\)), метоксиметан (\(C_2H_6O\)), диметиловый эфир этандиола (\(C_4H_{10}O_2\)) и другие, умеют создавать крепкие соединения с магнийорганическими веществами, которые содержат ковалентную связь C-Mg, литийорганическими веществами, содержащие взаимосвязь с литием, обладающие жесткими кислотами (катионы лития Li либо магния Mg).
Нарушение эфирной взаимосвязи допустимо при осуществлении влияния галогеноводородов, образованных из водорода и галогенов (элементов подгруппы фтора):
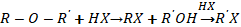
\(Ar-O-R+HX \to RX+ ArOH \)
Реакционный потенциал галогеноводородных кислот снижается в ряду:
\(HI > HBr > HCl\)
Нарушение эфирной взаимосвязи осуществляется при жестких условиях: с кислотами, обладающими высокой концентрацией, при нагреве.
Из алкиловых эфиров при нарушении эфирной взаимосвязи получаются органические соединения, содержащие одну либо больше гидроксильных групп, напрямую взаимосвязанных с насыщенным углеродным атомом, а также галогеноалкан. Далее спирт осуществляет реакцию с формированием галогеноалкана.
Алкилариловые эфиры расщепляются по взаимосвязи кислород-алкил, в итоге реагирования формируются гидроксибензол (\(C_6H_6O\)) и галогеноалкан.
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Ключевые свойства простых эфиров выражаются в их способности образовывать с иными соединениями однородные системы в сконцентрированной серной кислоте (\(H_2SO_4\)) и отделении оксониевых солей при невысоких температурных показателях.
Этоксиэтан используют в реакции Гриньяра как вещество, способное растворять другие твердые, жидкие либо газообразные вещества. Относительно к кислому магнию этоксиэтан представляется как основа. С положительным выходом реагенты Гриньяра обретают в фениловом водороде (\(C_6H_6\)) при наличии третичного амина \((C_2H_5)_3N\) в качестве основы.
Расщепление осуществляется в итоге реакции нуклеофильного замещения протонированного эфира ионом галогена. Таким образом осуществляется замена молекулы слабоосновного спирта.
Рисунок 1.
Первичная алкильная группа обладает стремлением к \(S_N2\)-замене, а третичная - к \(S_N1\)-замене.
Простые эфиры обладают возможностью образования крепких связей с жесткими кислотами Льюиса структуры 1 к 1 либо 1 к 2 – \(AlR_3\), \(AlBr_3\), \(BF_3\), \(SbF_5\), \(SbCl_5\), \(ZnCl_2\), \(SnCl_4\) и так далее.
Рисунок 2.
В роли оснований Льюиса, простые эфиры принимают участие в формировании соединений с галогенами. В соединении галоген занимает место акцептора, а простой эфир занимает место донора. Устойчивость соединения возможно проанализировать по спектрам поглощения в ультрафиолетовой зоне. В данной зоне возникает новый участок поглощения – участок переноса заряда.
В первый раз соли триалкилоксония извлечены немецким химиком-органиком Гансом Лебрехтом Меервейном, в конце 30-х годов XX столетия. Данные соли формируются при взаимосвязи простых эфиров с очень сильными алкилирующими агентами:
Рисунок 3.
В итоге взаимосвязи комплекса с диэтиловым эфиром (эфират трифторида бора, \(BF_3∙Et_2O\)) с хлорметилоксираном (\(С_3H_5ClO\)) легко образовывается триэтилоксонийборфторид (реакция происходит в абсолютном эфире):
Рисунок 4.
На сегодняшний день для того, чтобы получить соли триалкилоксония, осуществляют реакции эфиров с алкилами фторсульфонов либо с алкилтрифлатами.
Положительно заряженный ион триалкилоксония считается сильным алкилирующим агентом для каждого нуклеофила:
Рисунок 5.
Возможность простых эфиров создавать соли гидроксония применяются в органическом синтезе при разделении простых эфиров под воздействием иодистоводородной, бромистоводородной кислот, тригалогенидов бора.
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
При реакции замещения, в которой атаку осуществляет электрофил, в ароматическом кольце алкоксигруппа –OR осуществляет ориентирование в ортоположение, а также в параположение, и осуществляет активацию непосредственно кольца. В то же время активизация кольца алкоксигруппой происходит сильнее, нежели R, однако не так сильно, как –OH. При атаке в ортоположения и параположения формируется карбониевый атом или группа из нескольких атомов. Предполагают, что данный атом стабилизован вкладом структур I и II:
Рисунок 6.
Данные структуры достаточно стабильны, поскольку в этих структурах все атомы обладают цельным электронным октетом. Возможность кислорода осуществлять разделения более одной пары электронов с кольцом и производить аккумулирование положительных зарядов соответствует ключевому свойству простых эфиров.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




