







Рисунок 1. Расчет величин в термодинамике.
Определённые показатели в термодинамике устанавливают точное количество тепла, которое требуется подвести к газу либо отвести от компонентов при повышении давления изнутри, чтоб сохранить неизменяемыми температурные показатели либо объём.
Сегодня учёные фиксируют двенадцать коэффициентов термодинамики. Несложно продемонстрировать, что лишь 3 возможно считать независимыми. Оставшиеся 9 коэффициентов термодинамики возможно выразить непосредственно, используя три независимых коэффициента. Выбор трёх независимых коэффициентов термодинамики остаётся ещё произвольным. Остальные коэффициенты выражаются через отобранные благодаря формулам.
По данное причине, при отборе коэффициентов термодинамики часто следуют следующим представлениям: так как 3 независимых показателя в границах термодинамического метода нет возможности обнаружить, то их величины обязаны быть извлечены опытным путём либо из статистической физики.
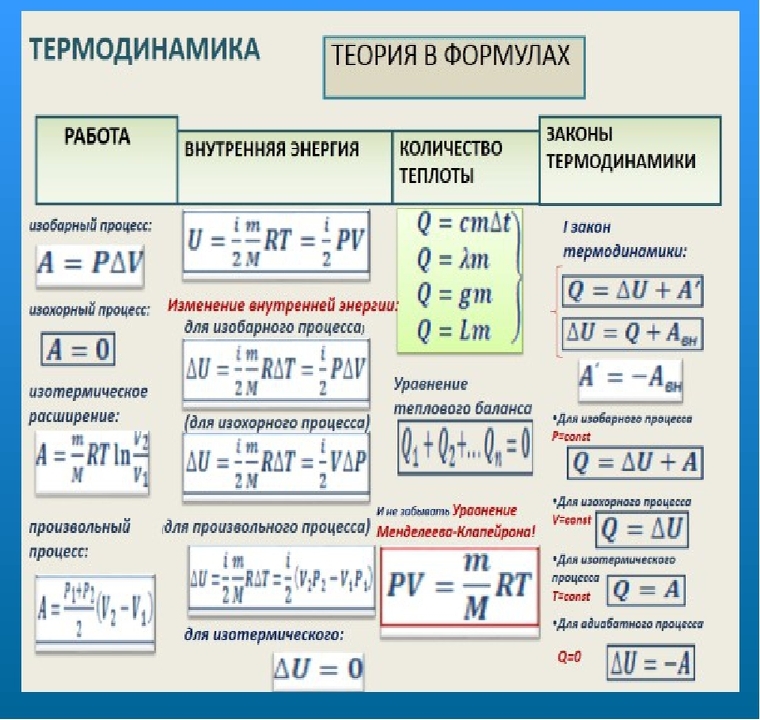
Рисунок 2. Термодинамическая теория в уравнениях.
Термодинамические функции физики определяют благодаря осуществлению экспериментальных опытов. Что относится к возможности их расчёта, то 2 несложно определить, когда первоначально найдена формула состояния материального объекта. В то время как зависимость третьего значения от температурных показателей можно отыскать исключительно методиками статистической физики. Вместе с тем данную зависимость от объёма находится в пределах термодинамических методик, когда известна формула первоначального состояния.
Когда показатель давления считается ключевой линейной функцией температурного показателя, что присутствует для идеального газа \(P ={RT\over V}\), а также для газа Ван-Дер-Ваальса, то
\(x = {d^2 V \over dT^2}=0, Cv = Cv(T).\)
Следовательно, на долю теории статистики кроме нахождения уравнения состояния остаётся вопрос установить быстро зависимость теплоёмкости от результирующих температурных показателей. Частные производные, которые входят в уравнения термодинамики устанавливают последующие характеристики структуры, а также обладают такими наименованиями: изобарный коэффициент расширения либо сжатия. Данный коэффициент описывают таким образом:
\(α = {1 \over v} [{dv \over dt}]\)
Термодинамический показатель упругости (изохорический коэффициент давления):
\(β = {1 \over p} [{dP \over dT}]\)
Последняя формула применяется в термодинамической дисциплине для нахождения значения β, ключевое предназначение которого применяется для физических объектов в конденсированном состоянии, поскольку произвести нагревание объекта без преобразования первоначального объёма практически нет возможности.
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
Каждая структура термодинамики характеризуется следующими показателями:
В каждой системе в обязательном порядке происходят физические явления. Данные явления являются либо равновесными, либо неравновесными, а также обратимыми или необратимыми. Когда в системе термодинамики определённая характеристика объекта не преобразовывается в определённом промежутке времени, т.е. данная характеристика будет полностью неизменной в каждой точке объёма, тогда данные явления считаются равновесными.
В неравновесных явлениях каждый параметр системы в обязательном порядке подвергается изменению в течение определённого промежутка времени без воздействия различных факторов снаружи, включая окружающую среду.

Рисунок 3. Термодинамические константы равновесий.
Обратимые явления изображают такие воздействия, в которых система возобновляется в изначальном состоянии, в то время, как необратимые явления, когда данная структура остаётся в своём изначальном состоянии. Термодинамические функции находятся в зависимости от следования самого явления. Функции, которые зависят от первоначального и окончательного положения системы, и не зависят от следования явления – это функции общего состояния; энтальпия, внутренняя энергия, энтропия, фугитивность и так далее являются важными термодинамическими свойствами.
При анализе технологических процессов либо проектировании оборудования преобразование данных свойств зачастую могут быть взаимосвязаны с показателями процесса, к примеру, с повышением температурных показателей жидкостных веществ либо газа в теплообменном устройстве. По данной причине, является очень важным производить расчёты преобразования данных температур.
Методики термодинамической системы можно разделить на две категории: экстенсивные и интенсивные. Экстенсивное свойство системы прямо пропорционально весу перемещающихся компонентов. А также, обладает аддитивностью, т.е. величины возможно суммировать меж собой: \(V, H, Uвн, S, G, F.\) Интенсивное показатели структуры находятся вне зависимости от массы и обладает свойством аддитивности: \(Q, A, T, P.\)
Давление является показателем состояния, определяемый силой, которая действует в физическом объекте, что в результате квалифицирует взаимное воздействие системы и средой извне. Температурные показатели в системе термодинамики устанавливают значение максимальной интенсивности теплового перемещения атомов и молекул.
Начальные температурные показатели системы отсчёта постоянно являются произвольными. В роли эталонного объекта возможно избрать не водяную массу, любое иное материальное вещество. Лишь бы его характеристики постепенно преобразовывались с изменением температурных показателей, легко воспроизводились, а также быстро и качественно измерялись.
Данная произвольность невольно ликвидируется, когда использовать термодинамическую шкалу температурных показателей, базирующуюся на втором законе термодинамики. Первоначальной физической точкой данной многофункциональной шкалы является величина довольно низкого температурного показателя – абсолютный ноль. Равновесие напряжения на электрохимической аппаратуре устанавливает чёткие затраты электрической энергии во время электролиза.
Падение первоначального напряжения в коммуникациях по обыкновению принимаются ориентировочно от 5% до 10% от всеобщей интенсивности структуры. Понижение напряжения на электрохимической аппаратуре является образцовым промежутком меж электродами с электропроводностью, которая является предельной.
\(ΔU = {J \over 2}P {1 \over s}\)
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
К термодинамическим значениям имеют отношение те значения, с которыми возможно произвести точные расчёты, применяя в экспериментах и опытах законы термодинамики, принимая во внимание обстоятельства, что система постоянно существует в равновесном состоянии. Отклонение системы именуется в физике поляризацией. Электрохимическая неустойчивая реакция считается гетерогенным процессом, и её скорость ограничивается одной из степеней:
Устанавливаемая довольно медленной этапом массопереноса поляризация является концентрационной. Когда сложным этапом оказывается этап разряда всеобщей ионизации, тогда поляризация обладает наименованием термодинамическим перенапряжением. Природа и предназначение этого показателя находится в зависимости от большого количества факторов.
Кинетический параметр является значением, которое можно найти в реальных условиях функционирования электрохимической структуры. Термодинамические коэффициенты предоставляют возможность чётко и правильно рассчитать взаимную связь меж максимальной работой каждого физического явления и теплотой структуры. В том числе термодинамические коэффициенты предоставляют возможность использовать законы термодинамики к фазовым переходам.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




