






1. Реакция спиртов
2. Механизм рассматриваемых реакций и особенности их протекания
3. Некоторые особенности взаимодействия
Гидроксильной группой принято называть структурный фрагмент молекулы \(ОН\), в которой атомы кислорода и водорода ковалентно связаны. Традиционно в химии носит так же название «спиртовая группа». Вообще же все химические реакции спиртов обусловлены именно наличием гидроксильной группы и строением углеводородной цепи.
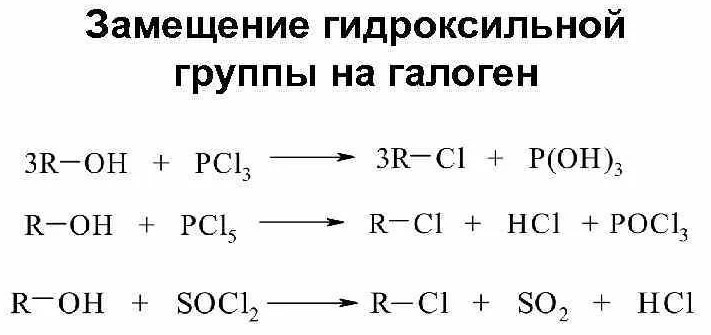
Одной из наиболее значимых реакций органического синтеза является замещение гидроксильной группы на галоген. Существуют вариации таких замещений, а полученные выходы колеблются в своих пределах.
Если спирты взаимодействуют с:
Для получения алкилгалогенидов принято проводить простую и легкую реакцию спирта с галогеноводородами. Есть несколько вариаций такой реакции: сухие газообразные галогенводороды пропускают через спирты или же спирты и кислоты нагревают вместе. Причём кислоты идут высокой концентрации.
Способность спирта к замещению гидроксильной группы снижается от третичного до первичного. \(ОН\) – группа так же выявляет разную активность при взаимодействии со спиртами. Так максимальная активность у йодоводорода, минимальная – у хлороводорода. Галогеналканы получаются, если спирты вступает в реакцию с \(ННal\). Существует ряд их возможности взаимодействия со спиртами: \(HI→HBr→HCl\).
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
При прямом воздействии фтороводорода замещение группы \(HO\) не происходит. Для окончательного результата приходится применять тетрафторид серы или селена. Таким же образом, н6аходясь в самом конце группы по способности к вступлению в реакцию, хлористый водород \(HCl\) может взаимодействовать со спиртами при присутствии \(ZnCl2\).
В то же время \(HI\) наиболее легко вступают в реакцию с концентрированной кислотой, например, соляной, причём даже при комнатной температуре. В результате образуются третичные алкид-хлориды. Выходы продуктов алкилгалогенидов при взаимодействии спиртов и галогенводородных кислот обычно чуть более 75%, но менее 90%.
Если мы рассматриваем механизмы реакции, мы помним, сто наиболее просто взаимодействие происходит с третичными спиртами, а труднее всего – с первичными спиртами. С третичными спиртами реакция протекает в основном по механизму \(Sn1\), что касается первичных спиртов, то реакция чаще всего идёт по механизму \(Sn2\).
Механизм \(Sn1\) включает в себя следующие этапы:
Пример: для того, чтобы трет-бутиловый спирт вступил в реакцию с хлористым водородом \(HCl\), достаточно комнатной температуры. Его реакция с первичными спиртами будет протекать лишь с применением кислот Льюиса в качестве катализаторов.
Замещение гидроксильной группы галогенами происходит в основном по нуклеофильному варианту механизмов взаимодействия. Это объясняется более лёгким образованием карбокатионов по сравнению с тяжёлым образованием нуклеофилов, в качестве основы, при условиях сильнокислой среды. Нуклеофилы \(RO\) являются основой для наступления реакции по механизму \(Sn2\).
На возможность и скорость нуклеофильного замещения влияет способность карбокатионов превращаться в алкены или изомеризоваться в условиях сильнокислой среды. Так, первичный неопреновый спирт будет вступать в реакцию с хлористым водородом по принципу механизма \(Sn1\), а не \(Sn2\) именно по упомянутой причине: существуют стерические препятствия для протекания реакции по второму механизму.
В результате, реагирование по механизму \(Sn2\) будет протекать выражено замедленно настолько, что молекула спирта уже успеет образовать оксониевое соединение. В результате просто превратится в карбокатион. В результате смещения (1,2-метльного) происходит процесс изомеризации первичного карбокатиона в третичный, что оценивается как более энергетически выгодно для реакции.
Реакции замещения гидроксильной группы галогеном ставят существенные требования к условиям проведения манипуляций.
Поскольку возможны существенные вариации итогового продукта:
При необходимой реакции спирта с галогенводородом в качестве катализаторов используют кислоты. Даже если водные растворы галогенводородов сами являются сильными кислотами, добавление серной кислоты ускоряет процесс образования алкилгалогенидов.
Действие кислот в качестве катализатора идёт по схеме: образование алкоксониевых ионов→данные ионы вступают во взаимодействие с ионами галогена → происходит нуклеофильное замещение. Лишь первичные спирты реагируют по механизму \(Sn2\). Третичные и вторичные вступают в реакцию по механизму \(Sn1\).
Для замещения третичного или вторичного спирта на галоген, необходимы три стадии:
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Подтверждением, что реакция протекает по механизму \(Sn1 \)заключается в перегруппировки алкидных радикалов. Галоген не всегда связывается с атомом углерода, который изначально был связан с гидроксильной группой.
Галогениды фосфора и хлористый тионил имеют свои уникальные особенности воздействия на спирты. Так, галогениды фосфора отличаются тем, что легко замещают гидроксильную группу спиртов на галоген. При взаимодействии \(PL3\) (которая образуется непосредственно в процессе реакции) и первичных спиртов получается сложный эфир, как побочный продукт. Поэтому, можно вводить в реакцию не конечный продукт, а фосфор и галоген. Таким образов в реакцию со спиртами вступают галогениды в момент образования. Реакция протекает по механизму нуклеофильному, лучше в присутствии пиридина.
При действии на спирты хлористого тионила \(SOCl2\), образуются хлоропроизводные, причем с высоким выходом. Так, реакция идёт по пути образования алкилхлорсульфида, через образование внутренней ионной пары. При отсутствии пиридина, реакция идёт по принципу \(Sn1\) и продукт имеет такую же конфигурацию реакционного центра.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




