






Практически любой объект, как органического мира, так и неодушевленной природы, невзирая на строение и многообразие данных объектов, включают в себя элементарные микрочастицы – атомы. Впервые научное высказывание по поводу атомов было сделано древнегреческим философом Демокритом Абдерским. Его принято считать одним из основателей атомистики, согласно которой чувственно воспринимаемые (материальные) вещи состоят из химически неделимых частиц. Непосредственно Демокрит установил, что атом является самой маленькой целостной частицей, формирующей вещество.

Лишь на закате XIX века были осуществлены выдающиеся открытия, которые сумели показать многосложность построения атома, с более маленькими элементарными частицами. Несмотря на это, данное объяснение обширно используется в нынешней научной деятельности, в частности, в физике и химии, невзирая на несоответствие его этимологии сегодняшнему восприятию о структуре атома.
Демокрит Абдерский заявлял, когда осуществить разделение яблока на две одинаковые части, после чего одну из данных частей разделить еще на две половинки, и производить разделение аналогично до тех пор, пока предмет исследования прекратит существование, как яблоко, тогда самая маленькая частичка будет являться в этой ситуации атомом яблока.
Древнегреческих ученых и философов, которые придерживались гипотезы о существовании подобных очень маленьких неразделимых частиц, именовали атомистами.
В нынешней научной деятельности проблема атомизма является открытой и на сегодняшний день. Определенная часть теоретиков высказываются за убеждения атомизма, но под атомами предполагают определенные базовые частицы, которые в последующем нет возможности поделить на части.
В основании квантовой теории атомного построения возможно произвести выделение таких основных принципов:
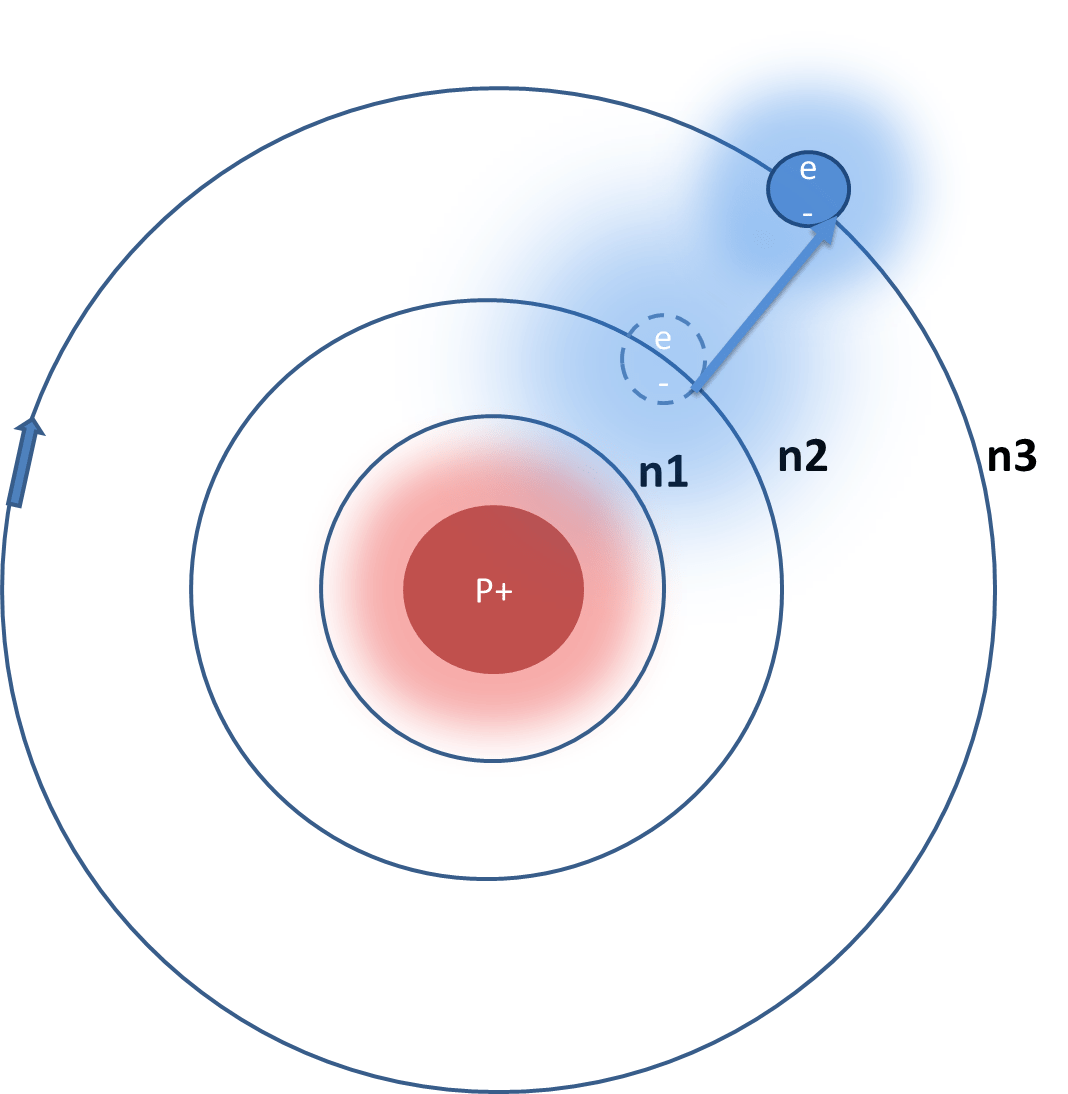
Есть смысл заметить, что пространство возле ядра, где, скорее всего, находится электрон, именуют орбиталью.
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Верная формулировка указанных выше положений в квантовой гипотезе атомного построения образовывают сущность обновленных представлений, которые осуществляют описание бесконечного перемещения микроскопических частиц в квантовой механике.
Самый большой вклад в формирование квантовой теории строения атома привнесли следующие ученые, которые являются основоположниками квантовой механики:
В итоге собственной научной деятельности все эти ученые в разное время был лауреатами Нобелевской премии по физике.
В начале XIX столетия английский физик и химик Джон Дальтон осуществил возрождение атомизма, как направления в физической науке, представив доказательства реальности наличия атомов. Ученый утверждал, что наименьшие частицы являются химическими элементарными компонентами, которые нет возможности вновь воссоздать, поделить на более маленькие компоненты либо уничтожить с помощью физических преобразований. Всякая химическая реакция имеет возможность лишь произвести изменения состояния соборности атомов.
Джон Дальтон предложил научному сообществу понятие «атомный вес». Далее, ученый впервые произвел расчеты атомного веса некоторого количества веществ по отношению к водороду, а также осуществил разработку таблицы их относительных координат, основав собственными научными трудами прекрасную базу атомной теории построения элементов.
Ученый с полным основанием обладает большим уважением среди известных физиков того времени. Джон Дальтон стал очень популярен с помощью собственных инновационных и уникальных трудов в различных областях познания.
Джон Дальтон осуществил открытие закона парциальных давлений, а также закон размеренного расширения газообразных веществ при нагреве. Им, также, осуществлено открытие закона растворяемости газообразных веществ в жидкостях, и произведено установление закона кратных отношений, найден процесс полимеризации по образу бутилена (\(C_4H_8\)) и этилена (\(C_2H_2\)).
В XIX столетии проблема внутреннего состава атомом не появлялась, поскольку данные микрочастицы было принято считать неразделимыми. В конце XIX столетии британский физик Джозеф Джон Томсон, изучая катодные лучи света, установил, что атомы всех химических веществ включают в себя лишь отрицательные заряды, которые именуются электронами. Большим достижением британского физика в сфере физики является аргументация того, что любое вещество, образовывающее катодные лучи, включены в состав атома и взаимно идентичны.
По заявлениям Джона Томсона, положительно заряженные частицы в атоме заполняют фактически весь объем данного микроэлемента и распространен полностью с одинаковой плотностью. Таким образом, в положительно заряженном пространстве располагается, как правило, одновременно некоторое количество электронов.
Квантовая гипотеза построения атома обладала большим числом формулировок и способов применения. Электроны, которые осуществляют вхождение в структуру атомов, в итоге критического веса не смогут полностью произвести изменения всеобщей траектории альфа-частицы. Рассеянность либо изменение направленности перемещения элементов, имеет возможность вызова исключительно положительно заряженной части атома с тяжелой массой.
Со временем выяснилось, что большое число альфа-частиц постоянно следует сквозь тонкий пласт металла, но вместе с тем фактически не претерпевает сдвигов в траектории перемещения. Определенное незначительное число частиц со временем претерпевает сдвиг на существенный угол, который может быть более 30 градусов. Данные взгляды послужили основаниями для выводов у некоторого количества физиков, что атом фактически пустотелый, и весь его положительный энергетический потенциал сконцентрирован в достаточно маленьком объеме. Данную часть атома в физике именуют атомным ядром.
Таким образом, возникла первая планетарная модель атома:
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
Но на основании этой модели нет возможности пояснить сведения о непосредственном наличии атома, а также его устойчивости. Так как беспорядочное перемещение электронов по орбитам осуществляется с регулярным и относительно большим ускорением. Быстро перемещающийся элемент по электродинамическим законам должен тратить энергию и со временем осуществлять приближение к ядру.
Законы микроскопического мира, а также квантовых теорий в начале XX века пока не были предложены научному миру. Нильс Бор впервые сумел произвести формулирование данных законов в форме трех своих постулатов, осуществляющих дополнение планетарной модели атома Резерфорда. Учение Нильса Бора со временем обусловило появление последовательной концепции перемещения микроскопических частиц, а также стремительное развитие квантовой механики.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




