






Термодинамика является научной деятельностью, которая исследует взаимные изменения разных видов энергии. Данная наука не осуществляет рассматривание вопросов, которые взаимосвязаны с микрофизическим инструментарием исследуемых процессов, и по данной причине ее можно отнести к феноменологической научной деятельности. База термодинамики заключается в основополагающих природных законах.
Описанные в термодинамических понятиях, они именуются началами либо законами термодинамики. Благодаря данным началам термодинамика удачно осуществляет решения различных задач в современной промышленности.
В термодинамике существует несколько основных законов термодинамики, к которым относятся:
К ключевым типам задач по термодинамике возможно отнести следующие:
Условие задачи:
Один моль одноатомного идеального газа изобарным образом осуществляет распространение от объема 5л до 10л под давлением в 202000 Па. Как преобразуется внутренняя энергия газа в таком явлении?
Решение задания:
Для одноатомного газообразного вещества i=3. Для внутренней энергии идеального газа отразим, определяя температурные показатели благодаря уравнению Клапейрона-Менделеева:
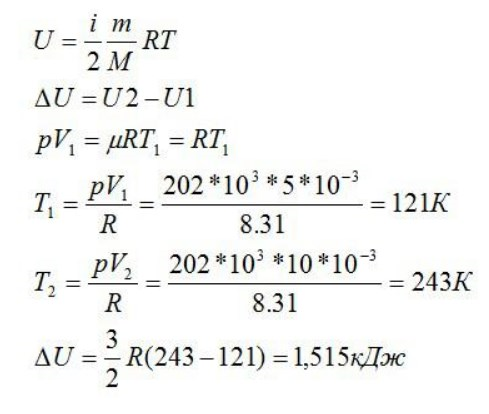
Результат: 1,515 кДж.
Условие задачи:
Газообразное вещество весом 2 килограмма заполняет объем 6 кубических метров и располагается при давлении одна атмосфера. Газообразное вещество изначально нагревается под стабильным давлением объема в 13 кубических метров, далее, осуществляется подогрев, обладая стабильным объемом давления 23 атмосферы. Рассчитать изменение внутренней энергии газа.
Решение задания:
Преобразование внутренней энергии рассчитывается благодаря равенству:
\(\Delta{U}={5m\over 2M}R(T_3-T_1)\)
Данное уравнение состояния возможно изменить. Для этого необходимо применить уравнение Клапейрона-Менделеева:
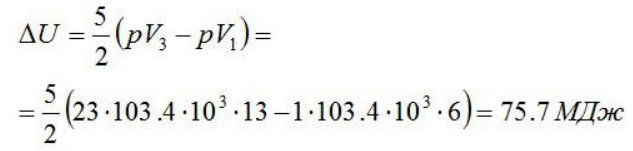
Результат: 75700000 Дж.
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
Условие задачи:
Установить количество теплоты, требуемое для расхода нагрева воздушной массы со стабильным давлением p = 0,2 МПа от t1 = 100°C до t1 = 500°C. Установить величину работы, выполняемую воздушной массой. Давление атмосферы приравнять к 101325 Па.
Решение задания:
В соответствии с нижеприведенной формулой:
\(q_p = c_{pm2}•t2 – c_{pm1}•t1\)
\(c_{pm1}=1,0061кДж/(кг*К);c_{pm2}=1,0387кДж/(кг*К)\)
Производим расчеты:
\(q_p=1,0387*500-1.0061*100=418.7кДж/К\)
Воздушную массу определяем из следующей формулы:

Следовательно,
\(Q_p=M_{qp}=5.63*418.7=2357кДж\)
Количество теплоты возможно рассчитать не исключительно по воздушной массе, но и по объему воздушной массы. В таком случае необходимо использовать формулу:
\(q_p = c'_{pm2}•t2 – c'_{pm1}•t1\)
\(c'_{pm1}=1,3004кДж/(м^3*К)\)
\(c'_{pm2}=1,3427кДж/(м^3*К)\)
Производим расчеты:
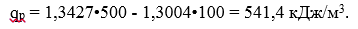
Объем воздушной массы приводим к обыкновенным условиям.
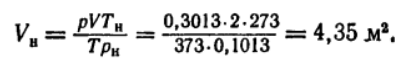
Следовательно,
\(Q_p=q_pV_н=541,4*4,35=2356Дж\)
Рассчитываем работу газообразного вещества:
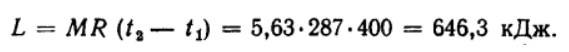
Условие задачи:
В замкнутом резервуаре располагается масса m1 = 20 грамм азота, а также масса m2 = 32 грамма кислорода. Рассчитать изменение ΔU внутренней энергии смешенного газообразного вещества, если охладить данную смесь на ΔТ = 28 K.
Решение задания:
Требуется установить число молей каждого газа в отдельности, а далее вычислить число вещества смешенного газообразного вещества.
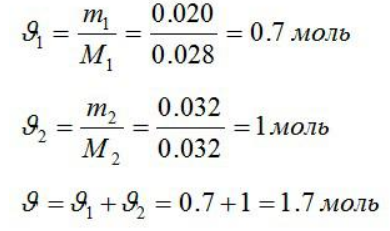
Вычисляем преобразование внутренней энергии:
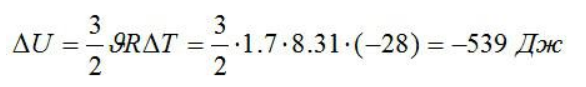
Результат: Внутренняя энергия газа уменьшится на 539 Дж.
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Условие задачи:
Азот весом 200 грамм распространяется изотермическим образом с температурными показателями 280 K. При этом объем газа повышается на 100%. Вычислить изменение ∆U внутренней энергии газа. Рассчитать осуществляемую газом работу при распространении. Рассчитать количество теплоты Q, переданное газом.
Решение задания:
Поскольку явление является изотермическим, тогда преобразование внутренней энергии приравнивается к 0. В свою очередь, работа приравнивается числу теплоты, которую получит газ.
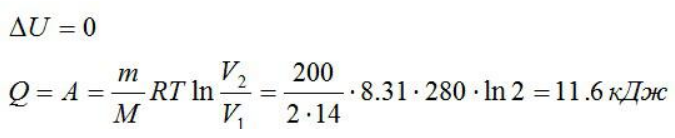
Результат: 0; 11600 Дж; 11600 Дж.
Условие задачи:
В емкость, которая содержит воду массой m1 = 1,5 килограмм при температуре t1 = +15°, впускают водяной пар массой m2 = 200 грамм при температуре t2 = 100°C.
Также даны значения:
Какая общая температура установится после конденсации пара согласно законам термодинамики?
Решение задания:
Количество теплоты, выделенное во время конденсации пара:
Количество теплоты, выделенное во время охлаждения водной массы, переданной из пара:
\(Q_2 = -сm_2(t_2-t)\)
Количество теплоты, переданное холодной водой:
\(Q_3 = сm_1(t-t_1)\)
Уравнение состояния теплового баланса:
\(Q_1+Q_2+Q_3=0\)
или
\(-rm_2-cm_2(t_2-t)+cm_1(t-t_1)=0\)
Осуществляем преобразование уравнения состояния теплового баланса и выражаем конечные температурные показатели t, t1, t2.
\(-rm_2-cm_2t_2+cm_2t+cm_1t+cm_1t_1=0\)
\(ct(m_1+m_2)=cm_1t_1+cm_2t_2+rm_2 \)
\(x = {c(m_1t_1+m_2t_2)+rm_2 \over c(m_1+m_2)}\)
\(t = {4200(1.5*15+0.2*100)+2.3*10^6*0.2 \over 4200(1.5+0.2)}=57^0C\)
Результат: Температурных показатель после конденсации паровой массы будет +57°C.
Условие задачи:
При изотермическом распространении, идеальным газом выполнена работа (A) 15000 Дж. Сколько количества теплоты передано идеальному газу?
Решение задания:
Поскольку процесс изотермический, то температура является постоянной, и внутренняя энергия газа считается неизменной, т.е. ∆U = 0. Тогда идеальный газ осуществляет работу за счет переданного ему количества теплоты, которая в данной ситуации равна работе:
\(Q=A\)
Таким образом, идеальному газу передано количество теплоты, приравненное выполненной работе:
Q = 15000 Дж.
Результат: Количество теплоты, переданное идеальному газу, составляет 15000 Дж. Это соответствует в данной ситуации выполненной работе.
Условие задачи:
Газообразное вещество располагается в поршневом цилиндре с профилем 200 квадратных сантиметров. После нагревания газообразного вещества, передав газообразному веществу теплоту 150000 Дж, поршень переместился на h = 0,3 метра. Каким образом преобразовалась внутренняя энергия газообразного вещества, если давление газообразного вещества не изменилось, и составляет 2•104 кПа?
Решение задания:
Математически первый закон термодинамики отражается следующим образом:
\(Q = ∆U + A\), где
Работу наружных силовых давлений, совершенную газообразным веществом, возможно рассчитать в соответствии с уравнением из механики. Работа будет представлена следующей формулой из механики:
\(A = p*S*h.\)
Подставляя уравнение вычисления работы в математическую формулу первого закона термодинамики, получаем:
\( ∆U = Q - A = Q - p*S*h = 1,5*105 - 2*10^7*2*10^{-2}*3*10^{-1} = 30 кДж\)
Результат: Исходя из первого закона термодинамики внутренняя энергия газообразного вещества поменялась на 30 кДж.
Идеальный тепловой двигатель совершает за один цикл работу 30 кДж. Если температура нагревателя 127 °C, а температура холодильника 27 °C, то какое количество теплоты отдано за один цикл холодильнику?
Решение задачи:
Коэффициент полезного действия идеального теплового двигателя η можно определять из системы уравнений:
η=A*Qн и η=Tн–Tх*Tн, где A- работа двигателя, Qн - количество теплоты,полученное от нагревателя, а Qх - количество теплоты, переданное холодильнику.
Подставляя в системы A=Qн-Qх, получаем:
A*Qх+A=Tн–Tх*Tн
Qх+A=A*Tн*Tн–Tх
Qх=A*Tн*Tн–Tх–A
Подставляем и решаем:
127∘C=400К
27∘C=300К
Qх=30⋅103⋅300400–300=90000Дж=90кДж
Ответ: за один цикл холодильнику передается 90 кДж теплоты.
В стеклянный сосуд, имеющий температуру 20 °C, налили горячую воду, масса которой 200 г и температура 100 °C. Спустя 5 мин температура сосуда с водой стала равна 40 °C. Какое количество теплоты терялось в единицу времени, если скорость охлаждения постоянна? Характеристики сосуда: масса 120 г, теплоемкость 840 Дж/(кг·К).
Решение задачи:
Дано: m1=120 г, t1=20∘ C, m2=200 г, t2=100∘ C, τ=5 мин, t=40∘ C, c1=840 Дж/(кг·К), необходимо найти N.
ΔQ=Q2–Q1, где ΔQ - теплопотери, Q1 – количество теплоты, полученное сосудом в результате теплообмена, Q2 – количество теплоты, отданное водой в результате теплообмена.
ΔQ=c2m2(t2–t)–c1m1(t–t1)
Удельная теплоёмкость воды c2 равна 4200 Дж/(кг·°C).
Так как в условии спрашивается “какое количество теплоты терялось в единицу времени”, то по сути нам нужно найти мощность. Её следует искать по формуле: N=ΔQτ
N=c2m2(t2–t)–c1m1(t–t1)
Подставляем известные данные и получаем: N=4200*0,2⋅(100–40)–840*0,12*(40–20)300=161,28Вт≈161Вт
Ответ: в единицу времени сосуд терят 161Вт теплоты.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




