






1. Понятие об изотопах
2. Кинетический изотопический эффект
3. Термодинамический изотопический эффект
4. Изотопический сдвиг
5. Применение изотопических эффектов
Исследуя радиоактивность элементов, ученые открыли явления, указывающие на то, на первый взгляд, абсолютно чистые химически атомы, в действительности представлены смесью атомов с одинаковым строением, но различных по массе.
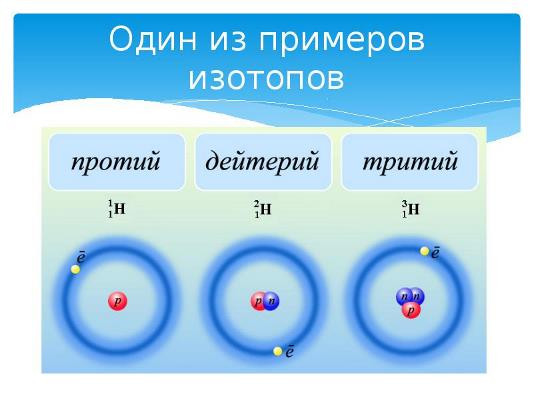
Измеряя атомные массы ученые обнаружили различные атомы того же химического элемента, имеющие отличие по массе, но с одинаковым зарядом. Такие атомы называют изотопами, а их атомные массы – изотопными. Замеры показывают, что изотопные массы в атомных единицах массы по значению приближаются к целым числам.
В основном у всех химических элементов наблюдается неизменный состав различных изотопов, а атомная масса химического элемента равна среднеарифметическому значению изотопных масс. Таким образом, химический элемент в чистом виде представляет собой смесь его изотопов с различающимися атомными массами.
Изотопические или изотопные эффекты представляют собой разность в свойствах изучаемого элемента, вызванные различиями в изотопных массах. Эти свойства присущи всем изотопам, кроме радиоактивных.
У большинства элементов изотопные массы не сильно отличаются, для них изотопные эффекты незначительны. Например, для элементов от Li до Ne разница изотопных масс равна не больше 35%, для тяжелых элементов – не больше 15%.
Различие масс изотопов значительное у химических элементов І периода таблицы Менделеева (H,He). Для водорода наибольшая разность равна 200%, а для гелия – 100%.
Структура электронных оболочек и энергетическое состояние электронов очень близки. Этим объясняется одинаковость в химических свойствах изотопов элемента. Но изотопы различаются в физико-химических свойствах. Из-за этого возникают изотопные эффекты, различают термодинамические и кинетические.
Сегодня ученым удалось обнаружить примерно 300 устойчивых изотопов и больше 100 радиоактивных.
В ядерной технике очень важным моментом есть деление различных изотопов химического элемента. Этим решается две проблемы: получение чистых изотопов и обогащение изотопных смесей избранными изотопами.
Термодинамическое неравновесие первоначальных изотопных соединений вместе с неравновесностью переходных состояний во время реакции предопределяют разность скоростей протекания химических реакций. В этом заключается принцип кинетического эффекта. Подобный эффект описывается соотношением постоянных скоростей химических реакций для различных изотопных соединений. Кинетические свойства изотопов определяются соотношением постоянных скоростей однотипных реакций, происходящих с участием разнообразных изотопных составов.
Стоит обозначить следующие моменты:
Разность изотопических свойств позволяет разделять изотопы и определять их количественное наличие в различных смесях. Данный анализ базируется на наличии некоторых изотопных эффектов. Таким образом, способы раздела, применяющие реакции изотопического обмена, базируются на термодинамическом изотопном эффекте. Кинетический изотопный эффект лежит в основе электрохимического метода создания тяжелой воды.
Разность изотопных масс провоцирует различие в некоторых изотопных свойствах, таких как вязкость, диффузия, плотность, проводимость, преломление, которые зависят от состава изотопной смеси.
При изменении энергетических уровней во время изотопной замены изменяются термодинамические свойства элемента, к примеру, температуры плавления, испарения, кипения, теплопроводность, теплоемкость и прочие.
Не нашли то, что искали?
Попробуйте обратиться за помощью к преподавателям
Стоит обратить внимание, что химические свойства элемента не зависят от состава изотопической смеси, так как изменение атомной массы не влияет на строение электронов, определяющих химические свойства. Но химические реакции зависимы от изотопического состава из-за того, что термодинамическое различие изотопических соединений приводит к неравномерному распределению изотопов во время равновесного изотопического обмена и адсорбции одной из форм на сорбенте.
Взаимосвязи масс изотопов с оптическими спектрами называются изотопическими сдвигами. Другими словами, это сдвиги уровней энергии и линий спектра атомов различных изотопов химического элемента один относительно другого. Изотопический сдвиг можно наблюдать, к примеру, при изучении колебательных или вращательных спектров молекул, состоящих из различных изотопов одного химического элемента.
Явление изотопического сдвига имеет ряд причин:
Размер изотопического сдвига и сверхтонкого расщепления практически одинаковые. Для легких элементов изотопический сдвиг получил название массового эффекта, потому что он вызван связью между энергией уровней и массой ядра.
Изотопический сдвиг является положительным в том случае, когда при росте массы ядра длина волны линии спектра стает меньшей. Для разделения изотопов с помощью лазера ориентируются на разность длин волн во время изотопического сдвига.
Наблюдается смещение уровней легких изотопов вверх, относительно более тяжелых уровней.
Рассмотрим примеры применения изотопических эффектов.
1) Учитывая, что химический элемент представлен смесью нескольких изотопов, определить изменение процесса сверхтонкого расщепления.
Решение: Учитывая, что для любого химического элемента спины и магнитные моменты ядер его различных изотопов не одинаковые, можно сделать вывод, что различные изотопы разнятся характеристиками сверхтонкого расщепления. Процесс наблюдений усложнен наложением явлений, происходящих отдельно в каждом из изотопов.
2) Описать суть метода изотопических индикаторов.
Решение: Метод изотопических индикаторов был предложен в 1913 году учеными Д.Хевеши и Ф.Панет. Он заключается в следующем: помеченный изотоп вводят в изучаемое вещество. Используются стабильные и радиоактивные изотопы. Суть метода базируется на одинаковости химических свойств изотопов изучаемого элемента. Таким образом, помеченный атом ведет себя одинаково с другими атомами изучаемого элемента.
Сложно разобраться самому?
Попробуйте обратиться за помощью к преподавателям
Они легко обнаруживаются, особенно если радиоактивные. Сложность данного метода заключается в том, что нужно учитывать возможность протекания реакции изотопического обмена. Подобные реакции могут привести к перераспределению помеченных изотопов и, следовательно, к их утрате. Применение стабильных изотопов является преимущественным в том плане, что они устойчивы и не нужно брать во внимание ядерное излучение. Но лишь у немногих элементов есть стабильные изотопы, и они сложнее обнаруживаются.
Базовыми методами анализа стабильных изотопов являются парамагнитный резонанс, спектрометрия и прочие спектральные методы.
Радиоактивные изотопы просто обнаруживаются, их возможно получить практически для любого химического элемента таблицы Менделеева. Однако, используя их, нужно учитывать радиационные эффекты, производящие влияние на течение исследуемых процессов. Такие изотопы обнаруживают при помощи их излучения, используя, к примеру, счетчик Гейгера.
Закажите подходящий материал на нашем сервисе. Разместите задание – система его автоматически разошлет в течение 59 секунд. Выберите подходящего эксперта, и он избавит вас от хлопот с учёбой.
Гарантия низких цен
Все работы выполняются без посредников, поэтому цены вас приятно удивят.
Доработки и консультации включены в стоимость
В рамках задания они бесплатны и выполняются в оговоренные сроки.
Вернем деньги за невыполненное задание
Если эксперт не справился – гарантируем 100% возврат средств.
Тех.поддержка 7 дней в неделю
Наши менеджеры работают в выходные и праздники, чтобы оперативно отвечать на ваши вопросы.
Тысячи проверенных экспертов
Мы отбираем только надёжных исполнителей – профессионалов в своей области. Все они имеют высшее образование с оценками в дипломе «хорошо» и «отлично».
Эксперт получил деньги, а работу не выполнил?
Только не у нас!
Безопасная сделка
Деньги хранятся на вашем балансе во время работы над заданием и гарантийного срока
Гарантия возврата денег
В случае, если что-то пойдет не так, мы гарантируем возврат полной уплаченой суммы
















































Заполните форму и узнайте цену на индивидуальную работу!




